바이러스연구실(임상시험센터 면역원성평가연구실)
바이러스연구실(임상시험센터 면역원성평가연구실)
실험실소개
1. 면역원성평가 연구실(Immunogenicity Evaluation Laboratory): 식품의약품안전처 지정 임상시험검체분석기관
면역원성평가연구실은 2018년 12월 7일 식품의약품안저전처로부터 <약사법 제34조의2제 1항> 및 <의약품 등의 안전에 관한 규칙 제 35조 제 5항>에 따라 임상시험검체분석기관으로 지정을 받았고 2019년 9월 1일부터 영남대학교 부속병원 임상시험센터 면역원성평가 연구실로 직제가 변경되었다.

가. SARS-CoV-2에 대한 면역원성 평가
SARS-CoV-2는 코로나-19(COVID-19) 질환을 유발하는 바이러스로 중국 우한에서 2019년 처음환자가 발생한 이후 전 세계로 급속히 확산되어 2020년 3월 WHO에서 Pandemic을 선언하였다. 코로나-19 첫 환자가 보고된 지 거의 2년 만에 전 세계에서 2억4천만 명 이상의 확진자와 500만명 이상의 사망자가 발생하였다. 본 연구실에서는 SARS-CoV-2에 대한 체액성 면역력과 세포성면역력을 측정하고 있다. 체액성 면연력인 중화항체는 Pseudovirus-based neutralization assay (PBNA)와 ELISA로 측정하고 세포성 면역력은 IFN-γ ELISpot으로 측정하고 있다. 2020년 11월에 개최된International Union of Microbiological Societies 학회에 코로나-19 완치자들의 장기면역 원성을 ELISA 항체가와 중화항체가, IFN-γ ELISpot, 일반 감기를 유발하는 HuCoV-OC43에 대한 IFA 항체가를 측정하여 건강한 성인과의 비교한 결과를포스터로 발표를 하여 Excellent E-Poster Presentation Award를 수상하였다. GC녹십자의코로나-19 혈장치료제의 2상 임상시험 검체에 대한 항체가 분석을 진행하였었고,고려대학교 의과대학 미생물학교실과 함께 질병관리본부의 '코로나-19 바이러스 중화항체 감염 방어능 평가 및 특성분석' 과제를 수행하였다. 현재 식품의약품안전평가원의용역과제인 ‘코로나19 예방백신의 세포성 면역원성 평가방법 개발 연구’를 진행하고 있다.
나. 수두 백신의 면역원성 평가(Evaluation of varicella vaccine immunogenicity)
수두는 수두-대상포진 바이러스(varicella-zoster virus: VZV)(Fig. 1)는 주로 소아에서 발열과 발진을 동반하여 나타나는 질병으로 전염력이 무척 강한 질환이다. 우리나라에서는 1988년부터 일본에서 수입된 수두백신을 선별적으로 사용하다가,1990년대 중반부터 국내에서도 백신이 생산되기 시작하였고 2005년 소아 기본예방접종에 포함되었다. 하지만 수두백신의 면역원성을 측정하는 방법이 국제적으로 표준화가 되어 있지 않고, 국내에서는 면역원성에 대한 평가 자료도 미비한 실정이었다.
수두는 일반적인 바이러스들과 달리 세포배양 시 세포 밖으로 나오는 바이러스가 거의 없어 중화항체가를 측정하기가 매우 어렵다. 따라서 수두에 대한 방어력을 측정하는 gold standard method는 fluorescent antibody to membrane antigen (FAMA) test (Fig. 2)이다. 우리 연구실은 2013년도부터 2015년까지 3년간 식품의약품안전평가원에서 "수두백신의 면역원성 평가 시험법 연구"에 대한 연구비를 지원받아 수두백신의 면역원성을 측정하는 Reference Laboratory의 기능을 할 수 있도록 실험 및 quality assurance 시스템을 구축하였다. 2016년도부터 2018년도까지 FAMA 방법과 glycoprotein ELISA로 새로 개발된 녹십자의 수두백신의 2상과 3상 임상시험검체 1600 건의 분석을 의뢰받아 완료하였으며 그 결과로 녹십자는 2020년 식약처로부터 배리셀라주로 의약품 승인을 받았다.
우리연구실은 FAMA와 glycoprotein ELISA 항체가를 측정하여 두 시험법간에 상관관계가 있는지, 백신 접종 전후 항체가가 얼마나 상승하는 지에 대한 연구하고 있다. 이 연구 결과는 새로운 수두 백신의 허가에 필요한 임상시험의 검체 분석에 사용될 뿐 아니라 국민면역도 등의 조사에 사용된다.
-
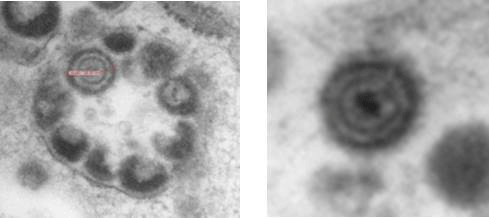
Fig. 1. Electron micrograph of varicella-zoster virus
-
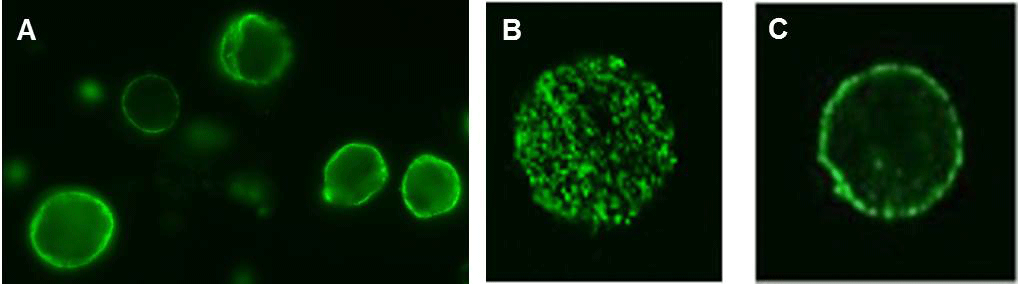
Fig. 2. Fluorescent antibody to membrane antigen (FAMA) test.
The images were taken with an Axioscope fluorescent microscope (A) and an a Leica SP2 confocal microscope (B, stacking image; C, single plane image)
다. 대상포진 백신의 면역원성 평가(Evaluation of zoster vaccine immunogenicity)
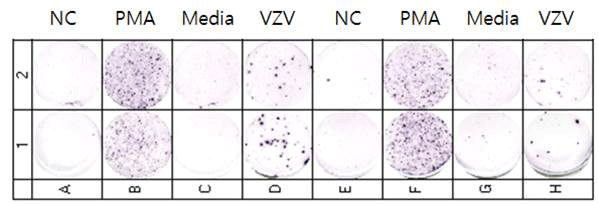
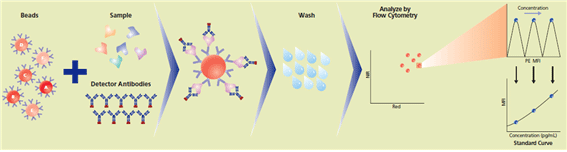
대상포진은 수두와 동일한 바이러스인 VZV에 의해 발생하나 발병 기전과 임상 증상이 전혀 다르다. 대상포진은 일단 우리 몸에 들어와 신경절에 잠복했던 VZV가 재활성되어 신경세포를 타고 다시 피부로 가서 수포와 통증을 유발하는 질병이다. 따라서 수두의 예방에는 혈액 내 중화항체가 방어력에 중요한 역할을 하는 반면, 체내에서 이동 시 세포 밖으로 거의 나오지 않는 대상포진의 경우 세포매개 면역력이 방어력에 매우 중요하다. 그러므로 대상포진 백신의 면역원성 평가는 세포매개 면역력을 측정해야 한다. 우리 연구실에서는 VZV에 대한 메모리 T 세포의 활성을 측정하기 위하여 IFN-γ ELISpot assay (Fig. 3)를 확립하여 건강한 성인과 백신을 접종받은 전후 성인의 면역원성을 측정하고 있다. 또한 T 림프구에서 분비되는 다양한 사이토카인을 동시에 측정하기 위하여 Cytometric bead array (CBA) 방법으로 IFN-γ 외에도 IL-2, IL-4, IL-6, IL-10, TNF 등을 동시에 측정하는 방법을 사용하고 있다(Fig. 4). 이 방법들은 새로운 대상포진 백신의 허가에 필요한 임상시험의 검체 분석에 사용될 뿐 아니라 국민면역도 등의 조사에 사용된다.
-
Fig. 3. ELISpot assay results.
-
가. 콕사키바이러스가 임신에 미치는 영향(Effects of coxsackievirus on pregnancy)
콕사키바이러스는 피코르나 바이러스과 (Picornaviridae)의 Enterovirus 속에 속하는 작은 바이러스로 중추신경, 심장, 폐, 췌장, 점막, 피부 등 다양한 조직에 감염이 된다. 성인에서는 대부분 가벼운 감기 증상으로 나타나나, 소아에서는 포진성 구협염 (Herpangina), 수족구병 (hand-foot and mouth disease), 수막염, 흉막통, 심근염, 심막염 등 다양한 질환이 발생된다.
콕사키바이러스에 대한 수용체인 coxsackievirus-adenovirus receptor (CAR)는 발생 중 태아의 뇌나 심장 등에 많이 분포(Fig. 5)하고 출생 후 급격하게 감소한다. CAR는 심장 발생에 필수적인 물질로 CAR knock-out 마우스는 발생 9~11일경에 심장 발생 및 혈관형성에 문제가 생겨 태내에서 사망한다.
-
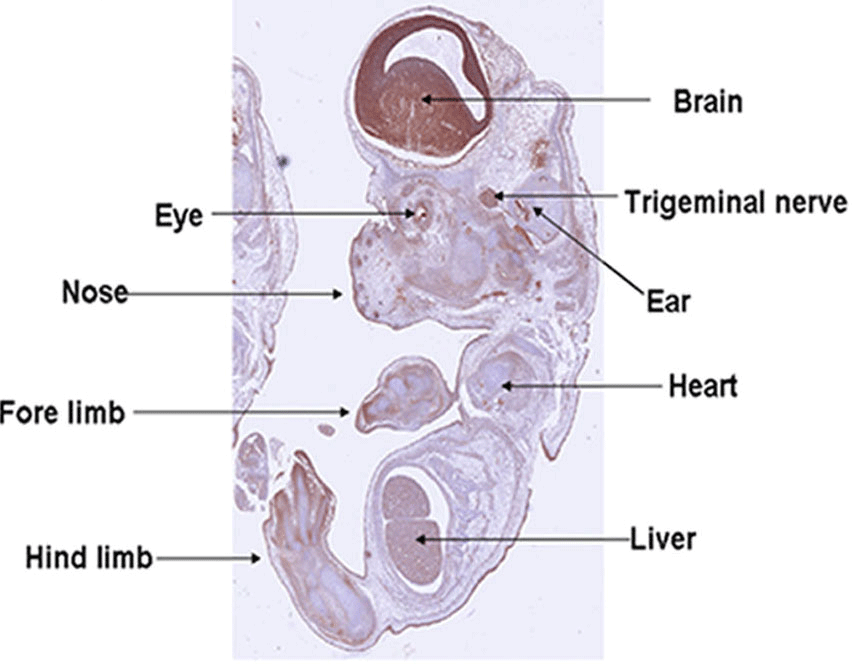
Fig. 5. CAR expression in 13 days old mouse embryo
유산(Miscarriage)
우리 연구실에서는 태아에서 뿐 아니라 여성의 생식기관인 자궁과 난소에서도 CAR의 발현이 매우 높음을 확인하였다(Fig. 6). 따라서 임신 초기의 ICR mouse에 콕사키바이러스 B3 (CVB3)를 감염시키면 유산율이 38.3%로 대조군에 비하여 8배가 높았다. 실제로 만삭과 조산환자에서는 1형 단순포진바이러스(Herpes simplex virus type I: HSV-1)가 주로 검출되는데 비하여 계류 유산 수태물의 57.1%에서 CVB3가 검출되었다. 또한 뇌류 기형이 있어 유산한 태아의 조직에서도 CVB1 유전자 및 바이러스 단백(Fig. 7)이 검출되었다.
-
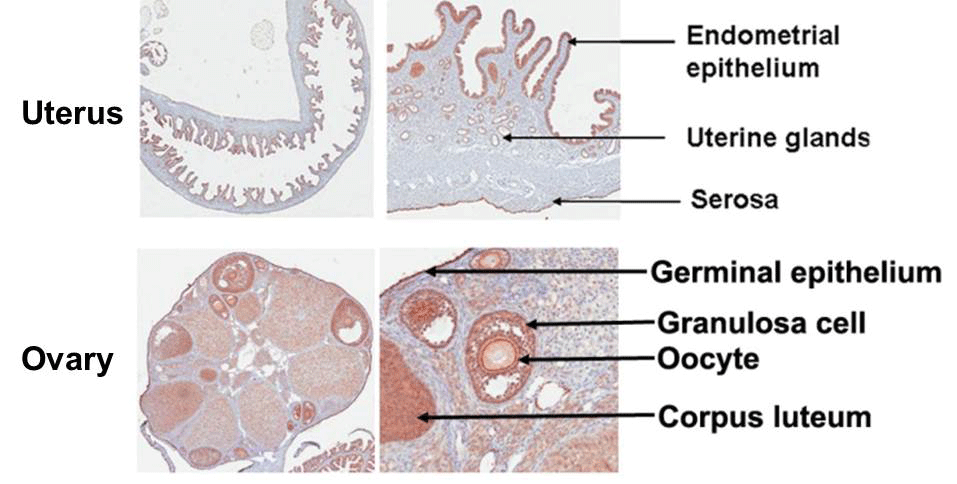
Fig. 6. Immunohistochemical analysis of CAR expression in mouse uterus and ovary.
-
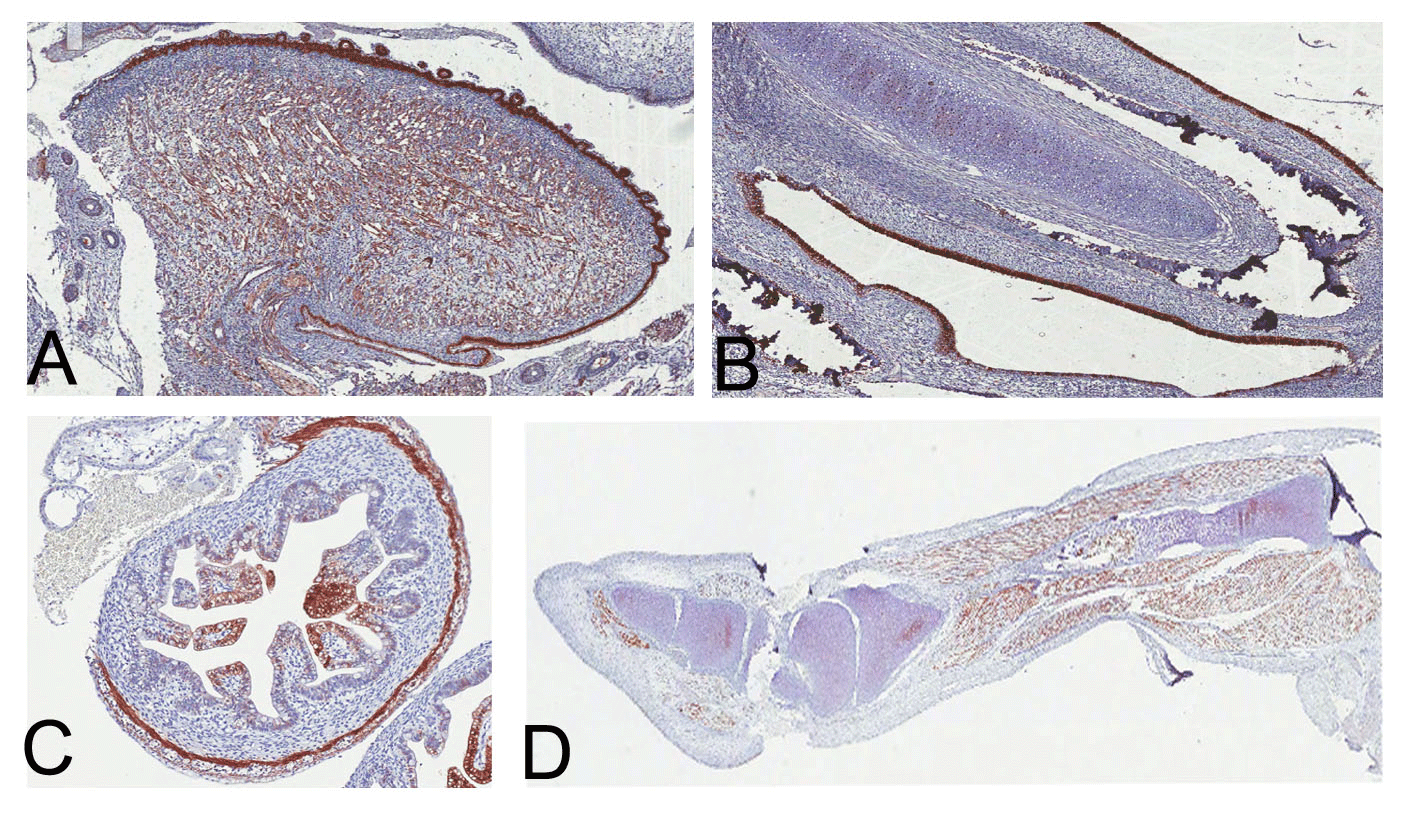
Fig. 7. The immunohistochemical analysis of the enteroviral VP1 capsid protein from tissues in an encephalocele case.
불임(Infertility)
우리 연구실에서는 난소의 granulosa cell에도 CAR의 발현이 무척 높은 것을 확인하였다. granulosa cell은 임신유지에 가장 중요한 호르몬인 estradiol이 합성되는 세포이다. ICR mouse에 CVB3를 감염 시킨 후 교배를 시키면 감염되지 않은 마우스의 임신율은 95%에 달하나 CVB3가 감염된 마우스의 임신율은 25%로 불임을 유발함을 확인하였다. 실제로 난소에서는 건강한 2차 난포의 수보다 atretic 한 2차 난포가 대조군에 비하여 유의하게 증가하였다. CVB3 가 감염된 마우스는 granulosa cell에서 estradiol 농도가 감소하였을 뿐 아니라 estradiol을 합성하는데 관여하는 효소인 aromatase의 mRNA 발현도 감소하고, 혈액 내 estradiol의 농도도 감소하였다. 또한 estradiol의 영향을 많이 받는 대퇴골의 골밀도(Fig. 8)도 감소되어 CVB3 감염이 불임에 영향을 미칠 수 있음을 확인하였다.
-
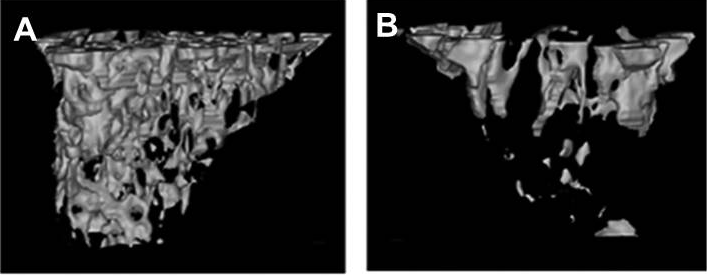
Fig. 8. MicroCT images of the tibia of mock (A) and CVB3-infected (B) mice at 28 dpi
나. 한탄바이러스의 출혈성 기전연구(Mechanism of hemorrhagic tendency induced by Hantaan virus)
신증후출혈열 (유행성출혈열)을 유발하는 한탄바이러스는 혈관내피세포에서 혈관 손상 시 지혈 작용에 가장 먼저 작용하는 von Willebrand Factor (vWF)발현을 감소시키고 (Fig. 9), 혈관 투과성에 관여하는 Angiopoietin-1의 발현을 감소시킨다. 또한 혈소판활성인자 수용체 (PAF-R)의 발현이 증가하고 신증후출혈열 환자의 혈액 내에서는 혈소판활성인자 분해효소 (PAF-AH)가 감소하여 출혈성 경향 및 혈관 내 응고 등의 병리 기전을 나타내는 것을 밝혔다.
-
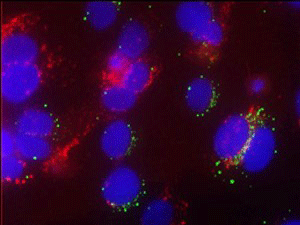
Fig. 9. HTNV infected HuVEC (HTNV, vWF)
■ 추후 연구 방향 및 연구 내용 (Future Research)
1. 백신 면역원성 평가 (Evaluation of vaccine immunogenicity)
우리나라에서는 최근 다양한 백신 개발이 진행 중이다. 백신의 효과를 측정하기 위한 지표로 면역원성 측정이 일차적 평가 대상이다. 대부분은 바이러스에 대한 중화항체를 측정하지만 세포매개면역력 등을 측정해야하는 경우 그 바이러스의 예방에 가장 중요한 biomarker를 찾는 것이 중요하다. 현재까지 대상포진 백신의 세포매개 면역력을 잘 대변하는 biomarker가 없는 실정이다. 따라서 대상포진에 대한 면역력을 잘 대변할 수 있는 새로운 biomarker를 찾아 면역원성 측정법을 구축하고자 한다. 또한 추후 다른 바이러스 백신들에 대한 면역원성 평가법도 구축 예정이다.
2. 임신에 영향을 미치는 바이러스 조사 (Survey for viral effects on pregnancy)
우리나라에서는 임신과 관련된 바이러스에 대한 연구가 거의 되어있지 않다. 따라서 많은 임산부 및 불임 부부들을 대상으로 검체를 확보하여 각종 바이러스에 대한 검사를 실시하여 실제 어떠한 바이러스가 유산이나 조산, 불임 등에 관여를 하는지에 대한 정보를 확보하고, 임신에 영향을 미치는 바이러스 지표를 개발하여 추후 백신이나 항바이러스제 개발에 필요한 근거를 마련하고자 한다.
3. CAR conditional knock-out mouse 제작(Establishment of CAR conditional knock-out mouse)
현재 심장에 특이하게 CAR 발현을 제한하는 knout-out mouse가 개발되어 있다. 성체에서 CAR는 난소나 고환에 많이 발현하므로 그 기능을 확인하기 위하여 난소와 고환에 특이하게 CAR 발현이 제한되는 knout-out mouse를 개발하여 CAR가 임신에 미치는 역할 등을 규명하고자 한다.



